残友生物是一家以基因与细胞科技为核心,集“产学研医”于一体的全产业链生物科技机构。公司下设生物科技研究院、生物实验室、医学检测中心、康复中心及诊所,致力于国际前沿生命科学技术的研究与转化应用。
公司汇聚了国内外顶尖生物医学专家,并组建了以全国高校医学、生物学、药学专业残障毕业生为主体的技术团队。目前已累计培训并就业300余名残疾人员工,涵盖实验、质检、质控等岗位,其中研发人员超过60人,全部持有细胞专业及相关能力认证,开创生物产业“试管+器皿”领域残疾人高技术培训与就业新模式。

公司拥有多项自主研发专利,覆盖细胞创新药核心领域。与中山大学、深圳大学、南方科技大学、四川大学华西医院、北京宣武医院、湖南湘雅医院、中山五院、北京大学深圳医院、深圳大学华南医院等多家医院、高校开展临床合作,并成立“联合实验室”“医学转化中心”等,共同参与多项行业标准制定,并且承担多项国家重点项目,荣获多项国家级奖项。

产业布局:“一中心、两基地”
深圳研发中心:位于南山区,占地面积3800㎡,涵盖生物实验室、检测中心、康复中心与诊疗中心。并获AABB、GMP(B+A)、CMA、CNAS等国际质量标准认证。


广州南沙综保区GMP药品生产基地:占地面积11000㎡,严格遵循国际GMP与AABB标准,具备承接全球药物研发与生产项目的资质。提供覆盖临床前研究至商业化生产的CRO/CDMO一体化服务,融合数字孪生、人工智能与区块链技术,实现药物全流程可视化与可追溯,支持国内外供应链高效协作。

防城港国际医学开放试验区GMP药品生产基地,总投资2.4亿元,规划建设面积15000㎡。基地立足广西,辐射东南亚与上合组织国家,聚焦细胞免疫治疗(CAR-T)、干细胞药物、ADC等前沿方向。配备自动化产线与人工智能系统,符合FDA、EMA、NMPA等多国监管标准,致力于建设“生物制造+人工智能”的精准医疗示范平台,打造“高价值、小切口”的应用示范窗口,以带动区域生物药产业升级与临床成果转化。

核心优势:以“中国速度”重塑CGT开发效率
在当前中国创新药生态中,“速度与效率”的极致结合是构建全球竞争力的核心。残友生物凭借独特的资源整合与模式创新,将这一优势转化为可量化、可复制的系统能力,显著降低综合成本,链接全球市场。
1. 研发速率:全流程高效转化
依托深圳研发中心的前沿探索与广州南沙、广西防城港生产基地的产业化支撑,构建生物创新药的全产业链平台,探索跨境交付、跨境支付、国际保险理赔等多元化支付体系,链接全球生物医药市场。
2. 全球(GMP)合规制造能力:公司严格遵循:FDA 21 CFR Part 11、EU GMP Annex 11、NMPA GMP等国际标准,具备多国申报与跨境交付能力。依托保税区“境内关外”功能区的独特优势,享受设备及原材料“免税保税”政策,有效降低生产成本,规避国际技术管制风险。
3. 效稳定的生物制药工程师团队:公司核心成员具备国际药企及先进实验室实战经验,取得AABB、ISO、中检院质量复核及细胞药物能力认证等多项国际资质。团队结构稳定、分工明确,具备以下显著优势:
高稳定性:核心人员长期任职,熟练掌握GMP体系下的精细化生产流程;
高一致性:能在严苛质量体系中保持批次间稳定,保障国际客户长期信任;
成本可控:生产组织效率高,人工成本低于行业平均水平。
凭借“良率高、质量好、成本低”的CDMO工程能力和体系化能力,被誉为“生物制药领域的台积电”。


4. 数智化能力:基于国际GMP法规和FDA等国际监管机构合规化生产应用场景,结合符合21 CFR Part 11认证的《残友生物制造全流程管理系统》产生的大数据,打造生物制造领域智能体应用。采用“模块化产线+柔性制造”模式,配备自主研发的“细胞药物工厂数字孪生平台”(已入选国家“十三五”科技创新成就展),通过AI工艺优化与区块链追溯系统,确保生产质量一致性与全流程可追溯。
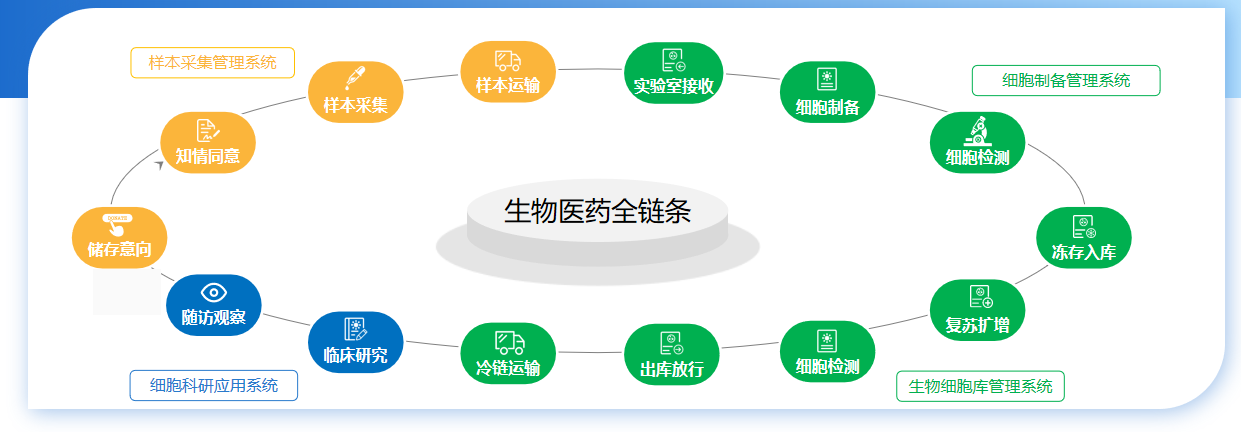
5. 人才与协同:深度参与的价值闭环
拥有一支由行业领军科学家、资深研发人员与专业稳定的残障生物工程师组成的复合型团队,全面覆盖细胞制备、载体研发与质量控制等关键环节。凭借对CGT研发逻辑的深刻理解,我们不仅能高效执行,更能主动参与研发设计、主导数据生成,构建“全流程研究与数据闭环”,实现同等项目的完成时间可比美国同行缩短50%以上。
6、标准化服务体系
以“原料药授权 + 临床代工 + 商业化生产”三轮驱动为核心,构建了分阶段、全链条的服务能力,具备以下显著优势:
1. 短期快速造血,稳健起步
通过标准化的原料药授权合作,可帮助客户快速完成技术转移与合规生产,在项目早期即形成稳定现金流,缩短回报周期,为中长期发展奠定资金与产能基础。
2. 中期能力深化,持续赋能
在药物研发的中期阶段,体系可承接临床样品生产与中试代工,依托标准化流程与核心产线,保障工艺稳定性与数据可靠性,加速客户临床试验进程,同时强化自身生产运营与项目管理能力。
3. 长期规模拓展,构建壁垒
体系支持从临床到商业化生产的无缝衔接,具备大规模产能与国际标准的质量体系,可承接全球订单,帮助客户实现产品全生命周期管理,最终形成规模化生产优势与品牌竞争力,建立行业壁垒。
商业模式
构建以“研发与生产双向赋能”为核心、“提升细胞与基因治疗全产业链资源利用效率”为目标的商业模式。通过四大核心板块的深度协同,系统性解决创新药企从早期研发到商业化生产全周期中面临的挑战,形成了强大的竞争壁垒和可持续的发展动能。
一、 CDMO服务:一体化与前瞻性布局
CDMO服务是残友生物商业模式的基石。其核心优势在于依托FDA、欧盟等国际认证及保税区政策,提供覆盖“临床前研究-临床试验-商业化生产”的全产业链服务,并为客户提供跨境生产、清关及全球供应链支持,高效承接来自欧美及新兴市场的订单,已与海内外多家药企实现商业化合作。
院企合作:与国内多家三甲医院构建了深度的合作关系。通过“院企合作”模式,精准对接前沿临床需求,高效贯通从实验室研发到产业化的关键路径,加速细胞与基因治疗等创新技术的转化与应用。并且构建了“临床需求引领研发方向、研发成果反哺临床应用”的闭环生态,显著增强了其作为CDMO企业在创新药,尤其是细胞与基因治疗领域的一体化服务能力与核心竞争力。
药企协同:与海内外多家药企的合作,展现了其作为战略合作伙伴的价值。合作不仅限于生产,更深入至“生物+数字”生态链共建、联合开发探索性临床等,深度融入全球创新网络。
差异化:在与国际巨头和本土头部企业的竞争中,残友生物凭借独特的“普惠商业模式”形成差异化:通过通用型技术降低成本,并结合残疾人就业获取政策支持,瞄准高端普惠市场。同时,其全产业链多管线布局有效分散了单一业务风险。


二、 原料药DMF授权:平台化创新的“全球加速器”
创新性地打造了“一次备案,中美双报”的干细胞原料药DMF(药物主文件)平台服务模式。该模式依托公司在细胞治疗领域的深厚技术积累与国际合规经验,旨在为全球创新药企提供高效、可靠的源头解决方案,显著加速细胞治疗产品的全球化开发进程。
①核心模式:“一次开发,中美双报”
核心是提供一站式的平台化备案授权服务,具体包含三个关键环节:
平台化备案:公司作为备案持有人(DMF Holder),利用成熟的干细胞工艺体系与符合中美标准的质量平台,主动完成原料药的研发、工艺验证及全套申报资料准备。
同步双报:关键突破在于可同步向中国国家药监局(NMPA)和美国食药监局(FDA)提交DMF备案,解决药企在不同监管区重复进行药学研究的痛点。
授权引用:药企在申报IND或NDA/BLA时,可直接授权引用此经过监管机构前置审核的DMF数据,省去重复开发环节,快速推进产品注册。
②核心价值:为药企研发“增效减负”
为合作药企带来三大核心价值:
显著提速:凭借经过验证的成熟平台,药企无需从零开始,整体申报周期预计可缩短30%-50%,助力前沿疗法快速进入临床,抢占市场先机。
大幅降本:药企可避免在细胞工艺开发、GMP车间建设等方面的巨额投入,通过平台化服务,单项目综合成本预计可降低约20%-30,使资源更能集中于核心研发。
降低风险:所引用的DMF资料已通过监管机构技术审核,资料质量与合规性有保障,能显著减少审评过程中的发补要求,提高申报成功率
三、 创新药申报:自主创新与技术赋能
公司通过自主创新项目强化其全链条能力。
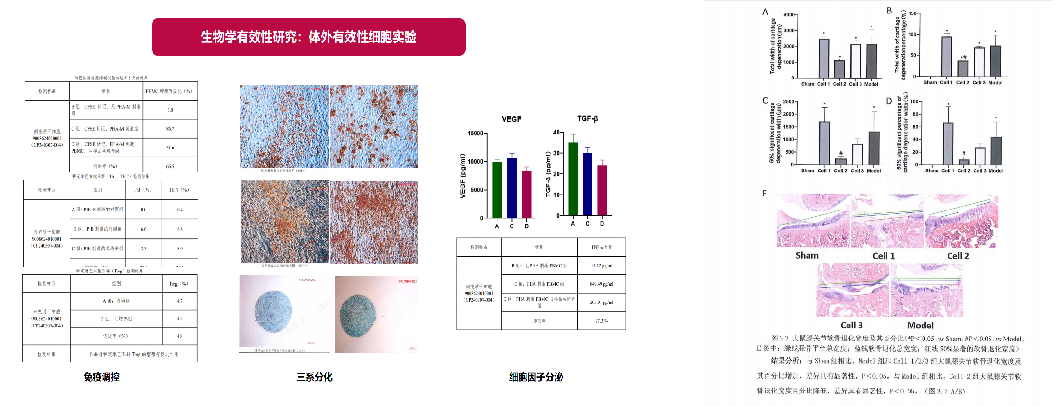
创新药管线:干细胞治疗膝骨关节炎注射液
自主知识产权的“脐带间充质干细胞治疗膝骨关节炎”IND项目。通过建立膝骨关节炎实验模型,系统评估脐带间充质干细胞在关节腔注射后的治疗效果及免疫调节机制,项目数据显示,间充质干细胞治疗可显著改善软骨缺损,当前已完成临床前研究和安评。
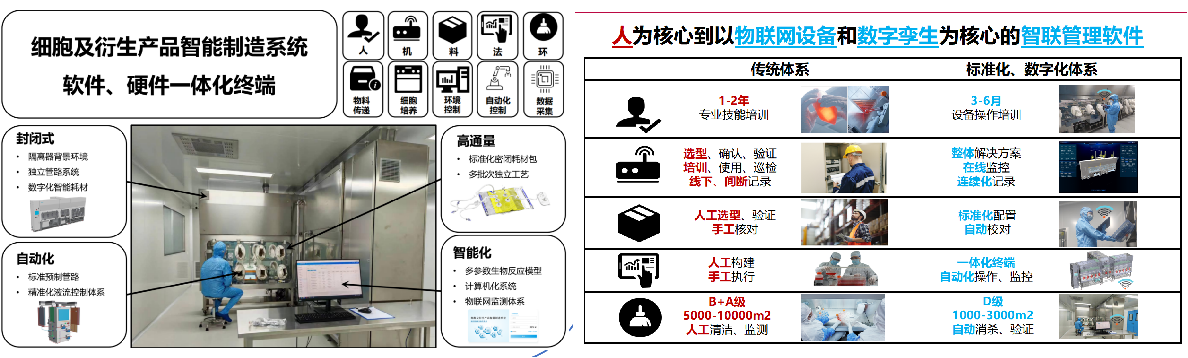
四、 细胞智能智造设备生产与销售
与中山大学共同研发、并荣获“国家生物药技术创新中心细胞疗法‘揭榜挂帅’项目”的《细胞及衍生品智能制造设备》及配套软硬件解决方案。提供覆盖药品生产全生命周期的交钥匙工程。
技术领先性:集成细胞职责设备和数字孪生技术,实现了从细胞采集到放行的全流程自动化、封闭式生产。其高通量自动分装和生物污染防控技术达到国际领先水平,直接解决了细胞制药行业中环境控制、物料检验等长期存在的瓶颈问题,确保了终产品质量的均一性和安全性,符合中国NMPA、美国FDA等严格法规要求。
残疾人就业与社会责任
作为中残联首批74家国家级残疾人大学生实习见习基地之一,残友生物为残疾人提供就业咨询、岗位适配、无障碍环境与专业培训一站式服务,涵盖细胞制备工程师、细胞检测工程师、QC质检员等重点岗位,并通过实训、资质认证等途径持续提升员工能力。
公司创新融合康复中心模式,结合基因治疗与罕见病防治经验,为残障员工提供康复评估、辅助器具适配、心理支持等全人关怀,助力其更好地融入社会。
